Les composés
On retrouve une centaine d'éléments dans le tableau périodique. Est-ce à dire qu'il n'existe qu'une centaine de différentes matières pures dans l'univers? Évidemment que non! Les éléments peuvent se combiner pour former des composés.
Parmi les composés, le plus étudié et le plus connu est certainement l'eau, dont la formule chimique est H2O. Mais que signifie cette formule?
On reconnaît deux symboles en lettres majuscules : H et O.
- Ces deux lettres indiquent la présence de l'hydrogène et de l'oxygène dans le composé
- On peut lire des indices qui suivent les symbole des éléments. Après H on voit l'indice 2 et après O, il n'y a pas d'indice.
- Le 2 après le H signifie que pour chaque molécule d'eau, il y a 2 atomes d'hydrogène.
- L'absence d'indice après le O signifie qu'il n'y a qu'un seul atome d'oxygène dans la molécule d'eau.
- Il y a donc deux fois plus d'atomes d'hydrogène que d'atomes d'oxygène dans l'eau .
Masse atomique (ou masse moléculaire) d'un composé
Puisque chaque molécule d'eau possède deux atomes d'hydrogène et un atome d'oxygène, la masse atomique totale d'une molécule d'eau est environ de 18 uma (valeurs arrondies à l'unité) :
- 2 atomes d'hydrogène x 1 uma par atome d'hydrogène = 2 uma
- 1 atome d'oxygène x 16 uma par atome d'oxygène = 16 uma
- masse totale = 2 uma + 16 uma
- masse atomique d'une molécule d'eau = 18 uma.
Analyse de formules chimiques - autres exemples
Sel de table : NaCl
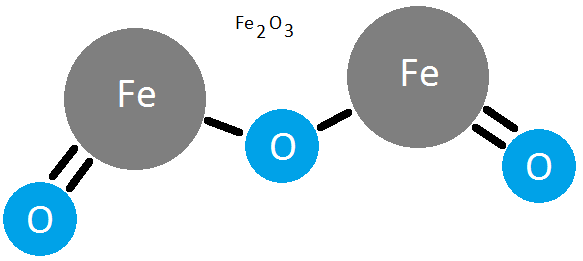
Rouille de fer : Fe2O3
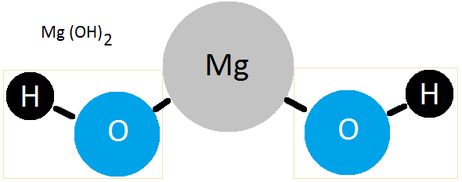
Lait de magnésie - médicament anti-acide : Mg(OH)2
Glucose - sucre produit par la photosynthèse : C6H12O6
Octane - essence d'automobile : C8H18
NaCl (chlorure de sodium)
- La formule indique deux symboles (chaque symbole débute par une lettre majuscule) : le sodium (Na) et le chlore (Cl)
- Les indices suivants chaque symbole indiquent la présence d'un seul atome de Na et un seul de Cl.
- La masse atomique du sodium est de 22,99 uma et la masse atomique du chlore est de 35,45 uma.
- 1 atome de sodium x 22,99 uma par atome = 22,99 uma
- 1 atome de chlore x 35,45 uma par atome = 35,45 uma
- la masse moléculaire du NaCl est donc de 58,44 uma
|
Le composé Fe2O3 a une quantité relative de 2 atomes de fer pour 3 atomes d'oxygène et sa masse moléculaire est de 159,687 uma.
Mg(OH)2 (hydroxyde de magnésium)
|
Le composé Mg(OH)2 a une quantité relative d'un atome de magnésium pour 2 atomes d'oxygène et 2 atomes d'hydrogène et sa masse moléculaire est de 58,3188 uma.
C6H12O6 (glucose) et C8H18 (octane)
- le glucose se compose d'une quantité relative de 6 carbone pour 12 hydrogène pour 6 oxygène avec une masse de 180,158 uma.
- l'octane a une quantité relative de 8 carbone pour 18 hydrogène et une masse moléculaire de 114,231 uma.
|
Exercices corrigés et autres renseignements sur les composés
|
| ||||||||||||