Classification des éléments

Dimitri Mendeleïev, un scientifique russe, a publié en 1869 ses travaux sur la classification périodique des éléments. Avant lui, on n'était pas arrivé à organiser les éléments d'une manière logique permettant de faire des prédictions sur les propriétés des éléments.
Pour développer sa classification, Mendeleïev a préparé des fiches sur lesquels il a inscrit les caractéristiques de tous les éléments connus à son époque. Il a placé les éléments dans une colonne en ordre de masse atomique. À ce moment, le premier modèle atomique de Thomson n'avait pas encore vu le jour - 1897 - et que les particules subatomiques n'étaient pas connues. On classait donc les éléments en ordre de masse atomique depuis le modèle atomique de Dalton de 1808.
Pour développer sa classification, Mendeleïev a préparé des fiches sur lesquels il a inscrit les caractéristiques de tous les éléments connus à son époque. Il a placé les éléments dans une colonne en ordre de masse atomique. À ce moment, le premier modèle atomique de Thomson n'avait pas encore vu le jour - 1897 - et que les particules subatomiques n'étaient pas connues. On classait donc les éléments en ordre de masse atomique depuis le modèle atomique de Dalton de 1808.
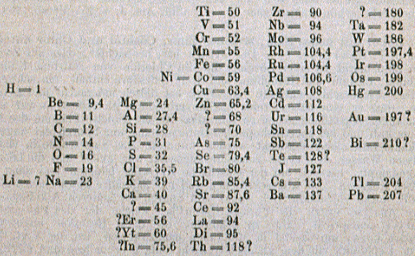
Dans une colonne, Mendeleïev place l'hydrogène, le béryllium, le bore, ... Il place le magnésium sur une deuxième colonne à côté du béryllium car les caractéristiques étaient similaires. Il place ensuite les éléments suivants sous le magnésium et s’aperçoit que les caractéristiques des éléments correspondaient bien à celles des éléments de la première colonne : L’aluminium était similaire au bore, le silicium au carbone, etc. Il continue à placer les éléments connus pour se rendre compte que les caractéristiques des éléments reviennent de manière périodique lorsqu'on place les éléments par ordre de masse. Lorsque les caractéristiques d'un élément ne correspond pas à ceux d'une même ligne, il laisse des espaces vides. Il prévoit ainsi que des éléments non découverts se trouvent à ces endroits.
Mendeleïev a vu juste. Après la découverte du proton, on a ordonné les éléments en ordre de numéro atomique plutôt que de masse atomique. Le tableau de Mendeleïev a été retravaillé par d'autres scientifiques. On l'a retourné pour placer les éléments aux caractéristiques communes dans une même colonne au lieu d'une même ligne (famille d'éléments). De nouveaux éléments ont été découverts pour remplir les trous laissés par Mendeleïev. Les caractéristiques de ces éléments correspondaient presque parfaitement aux prévisions de Mendeleïev.
Après les travaux de Bohr, on a compris que la périodicité des caractéristiques provenait de la configuration des électrons dans l'atome. Le nombre d'électrons de valence (électrons sur la dernière couche) est en grande partie responsable des caractéristiques physiques et chimiques des éléments. Le nombre d'électrons de valence dans une même famille d'éléments est constante. Par exemple, tous les éléments de la première colonne du tableau (famille des métaux alcalins) possèdent un seul électron de valence. Cette caractéristique profère aux éléments de cette famille leurs propriétés chimiques, dont leur grande réactivité avec l'oxygène et l'eau, tel qu'illustré dans cette vidéo trouvée sur Youtube.
Mendeleïev a vu juste. Après la découverte du proton, on a ordonné les éléments en ordre de numéro atomique plutôt que de masse atomique. Le tableau de Mendeleïev a été retravaillé par d'autres scientifiques. On l'a retourné pour placer les éléments aux caractéristiques communes dans une même colonne au lieu d'une même ligne (famille d'éléments). De nouveaux éléments ont été découverts pour remplir les trous laissés par Mendeleïev. Les caractéristiques de ces éléments correspondaient presque parfaitement aux prévisions de Mendeleïev.
Après les travaux de Bohr, on a compris que la périodicité des caractéristiques provenait de la configuration des électrons dans l'atome. Le nombre d'électrons de valence (électrons sur la dernière couche) est en grande partie responsable des caractéristiques physiques et chimiques des éléments. Le nombre d'électrons de valence dans une même famille d'éléments est constante. Par exemple, tous les éléments de la première colonne du tableau (famille des métaux alcalins) possèdent un seul électron de valence. Cette caractéristique profère aux éléments de cette famille leurs propriétés chimiques, dont leur grande réactivité avec l'oxygène et l'eau, tel qu'illustré dans cette vidéo trouvée sur Youtube.
|
|
vidéo : sodium dans l'eau
On trouve plusieurs vidéos sur Youtube présentant la réaction entre un métal alcalin et l'eau. Cette vidéo présente la réaction entre le sodium et l'eau. |
Tableau périodique des éléments
Le tableau périodique est donc organisé selon
- l'ordre des numéros atomiques des éléments (nombre de protons dans le noyau)
- configuration électronique des éléments (nombre d'électrons et niveau de valence des électrons)
- Le premier élément est l'hydrogène, un gaz ayant un proton et un électron de valence se situant sur le premier niveau d'énergie. On appelle « électrons de valence » les électrons se situant sur le niveau le plus éloigné du noyau. Dans le cas de l'hydrogène, puisqu'il n'y a qu'un seul électron (à son état neutre), l'électron de valence se trouve sur le premier niveau.
- L'élément suivant est l'hélium qui possède deux protons et deux électrons de valence se situant sur le premier niveau d'énergie. Puisque le premier niveau ne peut accueillir que deux électrons, ce niveau est complet ce qui profère à l'hélium des caractéristiques de stabilité qui fait que cet élément est très peu réactif avec les autres éléments.
- Le lithium possède trois protons et trois électrons, dont deux sur le premier niveau (période 1) et un seul sur le second niveau (période 2). Le lithium est un métal blanc, mou, très réactif. Bien qu'il n'est pas un gaz comme l'hydrogène, il possède un électron de valence et on le place sous l'hydrogène pour cette raison. Le lithium est le premier élément de la famille des métaux alcalins, la première colonne du tableau périodique (excluant l'hydrogène qui n'est pas un métal)
- Le quatrième élément, le béryllium, a quatre protons et quatre électrons dont deux électrons de valence sur le niveau 2. Puisque le béryllium a ses électrons de valence sur le même niveau que le lithium, on le place sur la même rangée (la même période). Le béryllium est le premier élément de la famille des métaux alcalino-terreux qui possèdent tous deux électrons de valence.
- On place ensuite les éléments possédant des électrons de valence sur la deuxième période : Le bore (3 électrons de valence), le carbone (4 électrons de valence), l'azote (5 électrons de valence), l'oxygène (6 électrons de valence), puis le fluor (7 électrons de valence).
- Le néon possède un niveau de valence complet avec 8 électrons. Bien que le nombre d'électrons de valence n'est pas celui de l'hélium, le néon possède des caractéristiques similaires - c'est un gaz très peu réactif car son niveau de valence est comblé. L'hélium et le néon font partie de la famille des gaz rares, comme les autres éléments de la dernière colonne du tableau périodique qui ont tous un niveau de valence complet.
- La troisième période est similaire à la deuxième période : huit éléments avec un nombre d'électrons de valence passant de 1 à 8 se situant sur le troisième niveau d'énergie (période 3). Le sodium possède des caractéristiques physiques et chimiques similaires au lithium, le magnésium est semblable au béryllium, etc. jusqu'à l'argon qui est un gaz rare peu réactif similaire au néon et à l'hélium.
- La quatrième période contient 18 éléments au lieu de 8. Les 10 éléments supplémentaires se retrouve dans la grande famille des métaux de transition au centre du tableau. Les éléments de cette période ne possède pas plus de 8 électrons de valence :
- Le potassium a un électron, le calcium en a deux, le gallium, comme l'aluminium et le bore en a trois... finalement, le krypton possède un niveau stable avec 8 électrons de valence.
- Le scandium possède 2 électrons de valence, mais un électron supplémentaire s'ajoute au niveau 3 : 2 sur n=1, 8 sur n=2, 9 sur n=3 et 2 sur n=4 pour un total de 21 électrons.
- Le titane possède deux électrons de valence sur le niveau n=4, mais deux électrons s'ajoute au niveau 3 : 2, 8, 10, 2 (total de 22 électrons)
- Les éléments suivants possèdent entre 1 et 2 électrons de valence sur le niveau n=4. Le nombre d'électrons sur le niveau n=3 augmente en conséquence. Le nombre maximal d'électrons sur le niveau 3 est 18 (10 électrons supplémentaires à 8 pour les 10 éléments se trouvant dans les métaux de transition)
- Les séries de 14 éléments des lanthanides (57 à 71) et des actinides (89 à 103) possèdent également un nombre d'électrons de valence variant de 1 à 2 électrons, mais on ajoute plus d'électrons sur les couches inférieurs.
Familles d'éléments
Parce que les éléments dans une même colonne ont généralement le même nombre d'électrons de valence, ceci procure aux éléments des propriétés physiques et chimiques semblables. Par exemple, tous les éléments de la colonne 1 possèdent un électron de valence lorsqu'ils sont neutres. À l'exception de l'hydrogène, tous les éléments sont des métaux blancs, mous (on peut facilement les couper avec un couteau) et très réactifs dans l'eau. De même, tous les éléments de la dernière colonne du tableau possèdent des propriétés similaires car ils possèdent tous un niveau de valence comblé avec 8 électrons (2 pour l'hélium). Ces éléments sont tous des gaz qui ne réagissent pas facilement avec les autres éléments puisque leur niveau de valence est déjà plein.
Les scientifiques appellent « famille d'éléments » le groupe d'éléments possédant les propriétés communes en raison d'un même nombre d'électrons de valences. Voici les noms de familles d'éléments les plus communs :
Plus sur les familles d'éléments
Métaux, non-métaux et métalloïdes
En plus des familles, les éléments sont groupés en trois grandes catégories.
Métaux
Les éléments à gauche du tableau périodiques possèdent des caractéristiques métalliques. Ils ont généralement peu d'électrons de valence qu'ils auront tendance à céder à d'autres éléments dans les réactions chimiques. Ils sont généralement des solides, durs, brillants, ductiles, conducteurs thermiques et électriques. Ils réagissent avec les acides en produisant de l'hydrogène. Ils peuvent s'associer à l'hydroxyde (OH) pour former des bases (LiOH, NaOH) en solution aqueuse.
Non-métaux
Les éléments à droite du tableau périodiques possèdent des caractéristiques non-métalliques. Ils ont généralement plus d'électrons de valence et auront tendance à accepter des électrons pour compléter leur niveau de valence lors de réactions chimiques. Ils sont généralement des gaz ou des solides friables, non ductiles, isolants thermiques et électriques. Associés à l'hydrogène (HF, HCl), ils forment des acides en solution aqueuse.
Métalloïdes
Séparant la gauche et la droite du tableau périodique, on retrouve des éléments appelés les métalloïdes. Leurs caractéristiques sont parfois métalliques, parfois non-métalliques, parfois entre les deux. L'exemple typique est le silicium dont les propriétés semi-conductrices ont permis le développement des micro-processeurs et de l'informatique. En plus du silicium, ce groupe se compose aussi des éléments suivants : le bore, le germanium, l'arsenic, l'antimoine, le tellure et l'astate.
Les scientifiques appellent « famille d'éléments » le groupe d'éléments possédant les propriétés communes en raison d'un même nombre d'électrons de valences. Voici les noms de familles d'éléments les plus communs :
- Métaux alcalins : première colonne (à l'exception de l'hydrogène qui est un gaz)
- Métaux alcalino-terreux : deuxième colonne débutant avec le béryllium (2 électrons de valence)
- Métaux de transition : colonnes 3 à 10, débutant avec le scandium jusqu'au zinc (généralement de 1 à 2 électrons de valence)
- Chalcogènes (aussi appelés sulfurides) : colonne 16 débutant avec l'oxygène (6 électrons de valence)
- Halogènes : colonne 17 débutant avec le fluor (7 électrons de valence)
- Gaz rares (aussi appelés gaz inertes et gaz nobles) : colonne 18 débutant avec l'hélium (couche de valence complète)
Plus sur les familles d'éléments
Métaux, non-métaux et métalloïdes
En plus des familles, les éléments sont groupés en trois grandes catégories.
Métaux
Les éléments à gauche du tableau périodiques possèdent des caractéristiques métalliques. Ils ont généralement peu d'électrons de valence qu'ils auront tendance à céder à d'autres éléments dans les réactions chimiques. Ils sont généralement des solides, durs, brillants, ductiles, conducteurs thermiques et électriques. Ils réagissent avec les acides en produisant de l'hydrogène. Ils peuvent s'associer à l'hydroxyde (OH) pour former des bases (LiOH, NaOH) en solution aqueuse.
Non-métaux
Les éléments à droite du tableau périodiques possèdent des caractéristiques non-métalliques. Ils ont généralement plus d'électrons de valence et auront tendance à accepter des électrons pour compléter leur niveau de valence lors de réactions chimiques. Ils sont généralement des gaz ou des solides friables, non ductiles, isolants thermiques et électriques. Associés à l'hydrogène (HF, HCl), ils forment des acides en solution aqueuse.
Métalloïdes
Séparant la gauche et la droite du tableau périodique, on retrouve des éléments appelés les métalloïdes. Leurs caractéristiques sont parfois métalliques, parfois non-métalliques, parfois entre les deux. L'exemple typique est le silicium dont les propriétés semi-conductrices ont permis le développement des micro-processeurs et de l'informatique. En plus du silicium, ce groupe se compose aussi des éléments suivants : le bore, le germanium, l'arsenic, l'antimoine, le tellure et l'astate.
Tableaux périodiques interactifs en ligne
Information sur les propriétés des métaux
