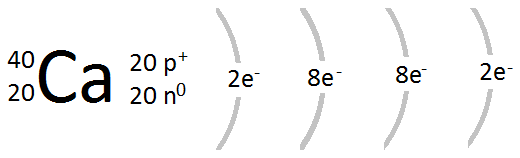Les éléments
La matière se compose d'atomes. Mais tous les atomes ne sont pas identiques. Il existe dans la nature une centaine de différents types d'atomes. Chaque type d'atome est un élément particulier.
Le mot élément réfère à la plus petite partie d'un tout. Nous savons que les atomes peuvent se diviser en plus petites particules que sont les protons, les neutrons et les électrons. Nous savons aussi que ces particules peuvent aussi être divisées en plus petites particules encore. Toutefois, mêmes si les différents types d'atomes sont composés de particules subatomiques, ils forment tout de mêmes des entités entières qu'on peut difficilement briser. C'est pourquoi on les appelle des éléments.
Exemple d'éléments - hydrogène et hélium
Le plus petit de ces éléments, le plus simplement constitué et aussi le plus abondant dans l'univers est l'hydrogène. La plupart des atomes d'hydrogène ne se composent que d'un seul proton autour duquel un électron unique tourne. Comme il ne possède qu'un proton, on lui donne le numéro atomique 1.
Le Soleil se compose principalement d'hydrogène. Par une réaction de fusion nucélaire, les atomes d'hydrogène du Soleil se combinent et forment un nouvel élément possédant deux protons et deux électrons qui les orbitent : l'hélium (le nom hélium provient du grec helios signifiant Soleil). L'hélium, avec ses deux protons, a le numéro atomique 2.
Chaque élément est donc différent des autres par le nombre de protons qui se trouvent dans son noyau. Le nombre de proton détermine donc la nature des atomes et représente le numéro atomique d'un élément.
Caractéristique des particules subatomiques
Mais les atomes ne se composent pas seulement de protons. Ils contiennent aussi des neutrons et des électrons. Le tableau qui suit brosse un portrait sommaire des trois particules subatomiques que nous étudions en 9e année
Le mot élément réfère à la plus petite partie d'un tout. Nous savons que les atomes peuvent se diviser en plus petites particules que sont les protons, les neutrons et les électrons. Nous savons aussi que ces particules peuvent aussi être divisées en plus petites particules encore. Toutefois, mêmes si les différents types d'atomes sont composés de particules subatomiques, ils forment tout de mêmes des entités entières qu'on peut difficilement briser. C'est pourquoi on les appelle des éléments.
Exemple d'éléments - hydrogène et hélium
Le plus petit de ces éléments, le plus simplement constitué et aussi le plus abondant dans l'univers est l'hydrogène. La plupart des atomes d'hydrogène ne se composent que d'un seul proton autour duquel un électron unique tourne. Comme il ne possède qu'un proton, on lui donne le numéro atomique 1.
Le Soleil se compose principalement d'hydrogène. Par une réaction de fusion nucélaire, les atomes d'hydrogène du Soleil se combinent et forment un nouvel élément possédant deux protons et deux électrons qui les orbitent : l'hélium (le nom hélium provient du grec helios signifiant Soleil). L'hélium, avec ses deux protons, a le numéro atomique 2.
Chaque élément est donc différent des autres par le nombre de protons qui se trouvent dans son noyau. Le nombre de proton détermine donc la nature des atomes et représente le numéro atomique d'un élément.
Caractéristique des particules subatomiques
Mais les atomes ne se composent pas seulement de protons. Ils contiennent aussi des neutrons et des électrons. Le tableau qui suit brosse un portrait sommaire des trois particules subatomiques que nous étudions en 9e année
|
nom de la particule
|
charge relative
|
masse relative
|
position dans l'atome
|
rôle
|
|
Proton
|
1 +
|
1
|
noyau
|
|
|
Neutron
|
neutre (0)
|
1
|
noyau
|
|
|
Électron
|
1 -
|
0 *
|
orbites
|
|
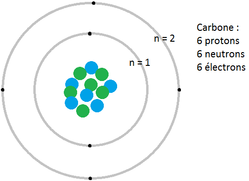 Modèle de Bohr du carbone
Modèle de Bohr du carbone
* La masse de l'électron n'est pas 0 car la matière ne peut pas être sans masse. Toutefois, sa masse relative est 1837 fois plus petite que celle du proton. Il s'agit d'une masse tellement insignifiante qu'on simplifie en lui donnant une masse de 0 par rapport à celle du proton.
Modèle de Bohr
Pour dessiner le modèle de Bohr d'un élément, on doit d'abord en connaître le nombre de protons, de neutrons et d'électrons.
Selon Bohr, les électrons se trouvent sur des couches précises représentant un niveau d'énergie précis. Le nombre d'électron sur une couche est limité :
Dans notre étude, en 9e année, nous ne tracerons que les modèles de Bohr des 18 premiers éléments. Ainsi le nombre d'électrons ne dépassera pas 18 au total et 8 sur le niveau n = 3.
Exemple : Le carbone
Pour dessiner le schéma de Bohr du carbone, il faut d'abord trouver le nombre de protons, de neutrons et d'électrons.
Il n'est pas pratique de représenter les atomes en dessinant chaque particule par un cercle. De fait, la forme réelle des particules n'est pas connue et il faut se rappeler que le modèle n'est qu'une représentation pour simplifier la réalité et l'atome n'est pas une structure en 2 dimensions. Si on veut représenter des atomes plus grands, ce serait laborieux de placer des dizaines de protons et de neutrons dans un noyau et de placer des dizaines d'électrons sur des cercles autour du noyau. De plus, le schéma produit deviendrait difficile à lire.
Modèle de Bohr
Pour dessiner le modèle de Bohr d'un élément, on doit d'abord en connaître le nombre de protons, de neutrons et d'électrons.
- Le nombre de protons est défini par le numéro atomique. Ainsi, l'hydrogène possède 1 proton, le carbone en a 6 et le calcium en a 20.
- La masse de l'atome se compose exclusivement de la masse des protons et des neutrons se trouvant dans le noyau (la masse des électrons est insignifiante). Pour simplifier, les scientifiques ont inventé l'unité de masse atomique et ont décidé que la masse du proton serait de 1 uma. Comme la masse du neutron est très proche de celle du proton, on lui attribue également une masse de 1 uma. Les scientifiques ont mesuré les masses atomiques des atomes de chaque élément. Par exemple, la masse atomique du magnésium est de 24 uma (arrondie). On sait que le magnésium possède 12 protons dans son noyau ce qui fournit une masse de 12 uma. La différence entre la masse de l'atome de 24 uma et celle des protons de 12 uma est de 12 uma. Cette masse provient des neutrons. Puisque chaque neutron possède une masse de 1 uma, il faut 12 neutrons pour atteindre une masse de 12 uma. Le magnésium possède donc 12 protons et 12 neutrons dans son noyau. Le phosphore a 15 protons et 16 neutrons (masse de 31 uma), l'argon a 18 protons et 22 neutrons (masse = 40 uma) et le nickel possède 28 protons et 31 neutrons (masse = 59 uma).
- Le nombre d'électrons doit être le même que celui des protons si l'atome a une charge neutre. Lorsqu'on crée un schéma de Bohr, on suppose que l'atome est de charge neutre. Le nombre d'électron est donc aussi donné par le numéro atomique de l'élément. L'aluminium a 13 protons, 14 neutrons et 13 électrons. L'azote a 7 protons, 7 neutrons et 7 électrons.
Selon Bohr, les électrons se trouvent sur des couches précises représentant un niveau d'énergie précis. Le nombre d'électron sur une couche est limité :
- La couche de niveau n=1 (la plus rapprochée du noyau) ne peut pas accueillir plus de 2 électrons.
- La couche de niveau n=2 (la couche suivante) ne peut pas accueillir plus de 8 électrons
- La couche de niveau n=3 (la troisième couche) ne peut pas accueillir plus de 18 électrons
- etc.
Dans notre étude, en 9e année, nous ne tracerons que les modèles de Bohr des 18 premiers éléments. Ainsi le nombre d'électrons ne dépassera pas 18 au total et 8 sur le niveau n = 3.
Exemple : Le carbone
Pour dessiner le schéma de Bohr du carbone, il faut d'abord trouver le nombre de protons, de neutrons et d'électrons.
- Le numéro atomique du carbone est 6, il y a donc 6 protons dans le noyau.
- La masse atomique du carbone est 12 uma (masse arrondie). Il y a donc 6 neutrons car il y a déjà 6 uma qui proviennent des 6 protons.
- Comme il y a 6 protons de charges positives, il faudra 6 électrons de charges négatives pour que l'atome soit neutre.
- On commence par remplir le premier niveau n = 1 qui ne peut prendre que 2 électrons.
- Il reste 4 électrons à placer. Le niveau n = 2 peut prendre un maximum de 8 électrons. Les 4 électrons qui restent peuvent donc se placer sur ce niveau.
- L'atome de carbone possède donc 2 électrons sur le niveau n = 1 puis 4 électrons sur le niveau n = 2.
Il n'est pas pratique de représenter les atomes en dessinant chaque particule par un cercle. De fait, la forme réelle des particules n'est pas connue et il faut se rappeler que le modèle n'est qu'une représentation pour simplifier la réalité et l'atome n'est pas une structure en 2 dimensions. Si on veut représenter des atomes plus grands, ce serait laborieux de placer des dizaines de protons et de neutrons dans un noyau et de placer des dizaines d'électrons sur des cercles autour du noyau. De plus, le schéma produit deviendrait difficile à lire.
Modèle de Bohr - représentation différente.
Cette manière de représenter les atomes fonctionnent bien pour les petits atomes contenant peu de protons. Pour les atomes plus gros, cette représentation donne des schémas difficiles à lire. par exemple, représenter un atome de calcium avec 20 protons et 20 neutrons dans le noyau (numéro atomique = 20 et masse atomique = 40 uma) donnerait un schéma très encombré et illisible.
Cette manière de représenter les atomes fonctionnent bien pour les petits atomes contenant peu de protons. Pour les atomes plus gros, cette représentation donne des schémas difficiles à lire. par exemple, représenter un atome de calcium avec 20 protons et 20 neutrons dans le noyau (numéro atomique = 20 et masse atomique = 40 uma) donnerait un schéma très encombré et illisible.
|
Pour simplifier le schéma de Bohr, on pourrait représenter les atomes plus gros, comme celui du calcium, d'une différente manière.
|
* Il y a un maximum possible de 18 électrons sur n = 3, mais chaque niveau se divise en sous-niveaux et il y a un chevauchement entre le premier sous-niveau de n = 4 et et le dernier sous-niveau de n = 3. Pour plus de renseignements sur la configuration électronique, suivez ce lien.
Il faut se rappeler que les schémas de Bohr ne sont que des modèles pour représenter l'atome en 2 dimensions. En réalité, on ne sait pas à quoi ressemble réellement un atome. Les orbites électroniques ne sont pas nécessairement circulaires (sphérique en 3 D) et les particules ne sont probablement pas des petites sphères. Les dimensions sont aussi non représentatives : l'atome est essentiellement vide et le noyau est minuscule en comparaison de l'espace totale occupée par l'atome. Les orbites ne sont pas aussi proches du noyau que dans les représentations qu'on en fait.
Modèle de Bohr et spectre électromagnétique
Lorsque des électrons sont excités par de l'énergie, ils accumule celle-ci et bondissent au niveau d'énergie plus élevé (transition). Ils deviennent alors instable et retombent à leur niveau de base. En retombant, ils émettent un paquet d'énergie (quantum) sous forme de photon et d'une longueur d'onde. Cette longueur d'onde peut être observée. Plus l'énergie est grande, plus la longueur d'onde tend vers le bas (les plus petites longueurs d'onde possèdent plus d'énergie). Moins d'énergie représente une longueur d'onde plus grande.
Les longueurs d'onde correspondant aux changements de niveau d'énergie se trouvent en fait dans le spectre visible (de 400nm à 700nm). Grâce au spectre électromagnétique, il est possible d'estimer l'énergie perdu par les électrons qui retournent à leur état de base et ainsi, de mesurer l'énergie de chaque orbite. C'est de cette manière que Bohr a pu déterminer la position des électrons et le niveau d'énergie de chaque orbite.
Les longueurs d'onde correspondant aux changements de niveau d'énergie se trouvent en fait dans le spectre visible (de 400nm à 700nm). Grâce au spectre électromagnétique, il est possible d'estimer l'énergie perdu par les électrons qui retournent à leur état de base et ainsi, de mesurer l'énergie de chaque orbite. C'est de cette manière que Bohr a pu déterminer la position des électrons et le niveau d'énergie de chaque orbite.
|
|
La vidéo à gauche montre comment des sels de différents métaux (chlorure de métal par exemple) émettent des photons avec différentes longueurs d'onde lorsqu'on excite les électrons en ajoutant de l'énergie (chaleur du feu).
Chaque couleur correspond à une longueur d'onde particulière et donc, à un niveau d'énergie particulier correspondant à la position des électrons. Pour apprendre davantage sur la spectroscopie : Introduction à la spectroscopie sur Khan Academy L'image en bas représente le spectre de différentes substances. Ces spectres sont habituellement obtenus en faisant passer de l'énergie électrique dans la matière ou dans un gaz de la matière jusqu'à ce que les électrons s'excite et émettent un rayonnement. Le rayonnement est alors décomposés avec un spectromètre. |
Isotopes - Pourquoi les masses ne sont pas des nombres entiers?
La masse d'un atome se compose de la masse des protons et de la masse des neutrons. La masse de ces particules est de 1 uma. Alors pourquoi la masse atomique n'est-elle pas un nombre entier? Par exemple, pourquoi le carbone a-t-il une masse de 12,011 uma et non de 12,000 uma? Y a-t-il des fractions de protons ou de neutrons dans le noyau du carbone?
Le nombre de protons et de neutrons dans le noyau d'un atome est toujours un entier. On ne peut pas avoir de fraction de proton ou de neutron. Dans le noyau de l'atome de carbone, il y a toujours 6 protons et tous les atomes qui ont 6 protons dans leur noyau sont des atomes de carbone. Toutefois, le nombre de neutrons dans le noyau n'est pas toujours de 6. Un petit nombre d'atomes de carbone qui se trouvent dans la nature possède un nombre différent de neutrons. La masse de ces atomes n'est donc pas de 12, mais pourrait être de 14 par exemple, si le nombre de neutrons est de 8 au lieu de 6. On dit alors que l'atome de carbone possède différents isotopes.
Il existe trois isotopes naturels du carbone.
La masse du carbone tient compte des différentes masses de tous les isotopes. En fait, la masse atomique correspond à la moyenne pondérée des masses de tous les isotopes naturels connus d'un atome en fonction de leur prévalence naturelle. Pour le carbone, puisque presque tous les atomes possèdent une masse de 12 uma et environ 1% possède une masse de 13 uma, la masse atomique du carbone est environ de 12,011 uma.
Le nombre de protons et de neutrons dans le noyau d'un atome est toujours un entier. On ne peut pas avoir de fraction de proton ou de neutron. Dans le noyau de l'atome de carbone, il y a toujours 6 protons et tous les atomes qui ont 6 protons dans leur noyau sont des atomes de carbone. Toutefois, le nombre de neutrons dans le noyau n'est pas toujours de 6. Un petit nombre d'atomes de carbone qui se trouvent dans la nature possède un nombre différent de neutrons. La masse de ces atomes n'est donc pas de 12, mais pourrait être de 14 par exemple, si le nombre de neutrons est de 8 au lieu de 6. On dit alors que l'atome de carbone possède différents isotopes.
Il existe trois isotopes naturels du carbone.
- Le plus fréquent est le carbone 12 possédant un noyau composé de 6 protons et de 6 neutrons. Cet isotope représente entre 98,9% et 99,0% de tous les atomes de carbone se trouvant dans la nature.
- L'isotope appelé le carbone 13 a un noyau constitué de 6 protons et de 7 neutrons. Il représente entre 0,96% et 1,15% des atomes de carbone.
- Finalement, il y a le carbone 14 avec 6 protons et 8 neutrons. Il n'y a que d'infimes traces de cet isotope dans la nature (le carbone 14 est utilisé pour dater des spécimens morts - comme les ossements de dinosaurs - car il se dégrade en carbone 13 et en carbone 12 à un rythme constant et connu. En connaissant la quantité de carbone 14 dans un spécimen, on peut savoir depuis combien d'année ce spécimen est mort)
La masse du carbone tient compte des différentes masses de tous les isotopes. En fait, la masse atomique correspond à la moyenne pondérée des masses de tous les isotopes naturels connus d'un atome en fonction de leur prévalence naturelle. Pour le carbone, puisque presque tous les atomes possèdent une masse de 12 uma et environ 1% possède une masse de 13 uma, la masse atomique du carbone est environ de 12,011 uma.
Ions - les atomes ne sont pas toujours électriquement neutres!
Comme pour le nombre de neutrons qui peut varié d'un atome à l'autre d'un élément, le nombre d'électron n'est pas fixe dans un atome. Les électrons peuvent assez facilement s'échapper ou s'ajouter à un atome, surtout si celui-ci n'a pas complété un niveau d'énergie avec tous les électrons possibles.
La configuration électronique fait en sorte que la couche électronique la plus éloignée du noyau ne peut accueillir qu'un maximum de 8 électrons (sauf pour la première couche qui ne peut en accueillir que 2). Par exemple, le fluor possède 9 électrons, dont 2 sur le niveau n = 1 et 7 sur le niveau n = 2. La dernière couche d'électrons du fluor pourrait accueillir un électron de plus pour être complète (8 électrons).
Le chlore a quant à lui un atome possédant 17 électrons, dont 2 sur n = 1, 8 sur n = 2 et 7 sur n = 3. Avec un électron de plus sur n = 3, cette couche serait aussi complète.
On appelle « électrons de valence » les électrons qui se trouve sur la couche la plus éloignée du noyau. On dit que le fluor et le chlore possède 7 électrons de valence lorsqu'ils sont électriquement neutre (aucune charge). On appelle « couche de valence » la couche contenant les électrons les plus éloignés du noyau. Les atomes ont tendance à rechercher une « couche de valence » pleine. Le fluor et le chlore vont donc chercher à obtenir un électron supplémentaire pour compléter leur couche de valence. Lorsqu'ils obtiennent cet électron, les atomes deviennent chargés électriquement car le nombre d'électron devient plus grand que le nombre de protons (10 électrons pour 9 protons dans le cas du fluor et 18 électrons pour 17 protons dans le cas du chlore).
Un atome qui possède une charge s'appelle un ion. le fluor qui obtient un électron de valence supplémentaire devient un ion négatif de fluor et on le note F-. De même, le chlore peut devenir un ion Cl-.
L'oxygène a 6 électrons de valence dans son état neutre. Il recherchera donc 2 électrons pour compléter sa couche de valence. Un atome d'ooxygène qui obtient 2 électrons de valence supplémentaires devient un ion O2-.
À l'autre bout du tableau périodique, les atomes ont très peu d'électrons de valence. par exemple, le lithium, le sodium et le potassium n'ont qu'un seul électron de valence. Le béryllium et le magnésium en ont 2. pour ces atomes, obtenir 6 ou 7 atomes supplémentaires est improbable. Ces atomes ont plutôt tendance à se débarrasser de leurs atomes de la couche de valence de manière à ce que leur dernière couche soit pleine.
Par exemple, le sodium possède 11 électrons : 2 sur n=1, 8 sur n=2 et 1 sur n=3. En se débarrassant de son électron unique sur n=3, le sodium a maintenant une dernière couche n=2 avec 8 électrons. On dira que cet atome est un ion positif du sodium, l'ion Na+.
De la même manière, l'atome de magnésium aura tendance à perdre ses 2 électrons de son niveau n=3. l'atome devient ainsi un ion Mg2+ puisqu'il possède toujours 12 protons positifs, mais seulement 10 électrons négatifs, soit une différence de 2 charges positives.
La configuration électronique fait en sorte que la couche électronique la plus éloignée du noyau ne peut accueillir qu'un maximum de 8 électrons (sauf pour la première couche qui ne peut en accueillir que 2). Par exemple, le fluor possède 9 électrons, dont 2 sur le niveau n = 1 et 7 sur le niveau n = 2. La dernière couche d'électrons du fluor pourrait accueillir un électron de plus pour être complète (8 électrons).
Le chlore a quant à lui un atome possédant 17 électrons, dont 2 sur n = 1, 8 sur n = 2 et 7 sur n = 3. Avec un électron de plus sur n = 3, cette couche serait aussi complète.
On appelle « électrons de valence » les électrons qui se trouve sur la couche la plus éloignée du noyau. On dit que le fluor et le chlore possède 7 électrons de valence lorsqu'ils sont électriquement neutre (aucune charge). On appelle « couche de valence » la couche contenant les électrons les plus éloignés du noyau. Les atomes ont tendance à rechercher une « couche de valence » pleine. Le fluor et le chlore vont donc chercher à obtenir un électron supplémentaire pour compléter leur couche de valence. Lorsqu'ils obtiennent cet électron, les atomes deviennent chargés électriquement car le nombre d'électron devient plus grand que le nombre de protons (10 électrons pour 9 protons dans le cas du fluor et 18 électrons pour 17 protons dans le cas du chlore).
Un atome qui possède une charge s'appelle un ion. le fluor qui obtient un électron de valence supplémentaire devient un ion négatif de fluor et on le note F-. De même, le chlore peut devenir un ion Cl-.
L'oxygène a 6 électrons de valence dans son état neutre. Il recherchera donc 2 électrons pour compléter sa couche de valence. Un atome d'ooxygène qui obtient 2 électrons de valence supplémentaires devient un ion O2-.
À l'autre bout du tableau périodique, les atomes ont très peu d'électrons de valence. par exemple, le lithium, le sodium et le potassium n'ont qu'un seul électron de valence. Le béryllium et le magnésium en ont 2. pour ces atomes, obtenir 6 ou 7 atomes supplémentaires est improbable. Ces atomes ont plutôt tendance à se débarrasser de leurs atomes de la couche de valence de manière à ce que leur dernière couche soit pleine.
Par exemple, le sodium possède 11 électrons : 2 sur n=1, 8 sur n=2 et 1 sur n=3. En se débarrassant de son électron unique sur n=3, le sodium a maintenant une dernière couche n=2 avec 8 électrons. On dira que cet atome est un ion positif du sodium, l'ion Na+.
De la même manière, l'atome de magnésium aura tendance à perdre ses 2 électrons de son niveau n=3. l'atome devient ainsi un ion Mg2+ puisqu'il possède toujours 12 protons positifs, mais seulement 10 électrons négatifs, soit une différence de 2 charges positives.
Exercices
| annexe_9_atome-configuration_des_particules.pdf | |
| File Size: | 222 kb |
| File Type: | |