Historique du modèle atomique et de la conception de la matière
L'être humain manipule depuis toujours la matière. Il s'est aussi demandé, très tôt dans l'Histoire, ce qu'est la matière. Voici des jalons marquants de l'exploration de cette question par l'être humain.
|
| ||||||||||||
Conception de la matière et développement scientifique avant le modèle atomique
|
Démocrite
Antiquité Grèce |
Il a énoncé l’idée que la matière se compose de particules indivisibles (ATOMOS) qu’il a appelé atomes et de vide. Démocrite se basait sur l'idée qu'une matière ne peut être divisée infiniment. Éventuellement on aboutit à une particule élémentaire indivisible. Le vide est nécessaire car sans lui, les particules ne pourraient pas se déplacer d'un point à un autre puisque tout l'espace serait occupé. Démocrite est un philosophe et n'appuie pas ses idées par l'expérimentation, mais par l'observation des phénomènes qui l'entoure et la déduction.
|
|
Aristote
Antiquité Grèce |
Aristote s'oppose à la théorie atomique de Démocrite. Grâce à sa notoriété, il impose plutôt la théorie des quatre éléments selon laquelle toute matière se compose, à diverses proportions, des éléments suivants :
|
|
Alchimistes
Antiquité Europe, Afrique, Asie |
Le mot « alchimie » provient de l'arabe « al-kīmiyā ». Les alchimistes ont une philosophie liée à l'expérimentation. Durant l'Antiquité, les alchimistes s'intéressent à la métallurgie (travaux sur les métaux) et à la pharmacie (travaux sur les substances médicinales, essentiellement de provenance végétale). Ils croient que les métaux poussent comme les plantes.
Les alchimistes antiques croient à la théorie des quatre éléments. Ils développent plusieurs techniques de laboratoire ainsi que des instruments tels que le bain-marie, attribué à Marie La Juive, une alchimiste du IIIe siècle. |
|
Alchimistes
Moyen-Âge Europe, Afrique, Asie |
Le développement de la verrerie par les alchimistes du Moyen-Âge permet l'accès à de nouvelles techniques et à de nouveaux instruments de laboratoire. Désormais, les alchimistes travailleront avec plus de précision dans des béchers, des fioles ou des ballons transparents pouvant résister à des chaleurs supérieures sans se déformer.
Les alchimistes de cette époque conservent leurs découvertes dans des grimoires codés et secrets ce qui ralentit l'avancement des découvertes scientifiques. ils sont en quête de richesse et pouvoir qu'ils obtiendraient par la transmutation des métaux en or, l'élixir de longue vie et autres pouvoirs mystiques et magiques. |
|
Antoine de Lavoisier
Fin 1700 France |
Lavoisier est surnommé le « père de la chimie moderne » parce qu'il s'oppose à la théorie des quatre éléments et à la philosophie de mysticisme de l'alchimie. Selon Lavoisier, les découvertes scientifiques doivent suivre une démarche scientifique rigoureuse basée sur l'hypothèse, l'expérimentation, l'observation, l'analyse des résultats et la conclusion.
Lavoisier croit que la matière se compose d'atome, mais il n'a pas les outils, à son époque, pour en faire une démonstration expérimentale. Il identifie 23 substances qu'il affirme être des éléments (substances pures ne pouvant être divisées en substances plus simples). Son épouse, Marie-Anne Pierrette Paulze, qui n'avait que 13 ans au moment de leur union, a assisté Lavoisier dans se travaux scientifiques. |
Le développement du modèle atomique
|
Ernest Rutherford
1871-1937 Nouvelle-Zélande |
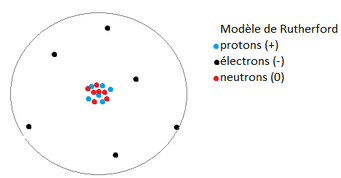
Rutherford confirme que l'atome se compose de protons et d'électrons, mais que ces particules ne sont pas organisées de manière aléatoire comme le laisse supposé le modèle du pain au raisin. Rutherford conçoit une expérience dans laquelle des particules positives (particules alpha) bombardent une mince feuille d'or autour de laquelle se trouve un écran cathodique. L'écran cathodique s'illumine en un point lorsqu'il est frappé par une particule positive. Il observe alors que la très grande majorité des particules alpha passent à travers la feuille d'or sans être déviées. Si l'atome était rempli de protons positifs, les particules alpha, elles aussi positives, auraient dû rebondir. Seulement certaines particules étaient déviées.
Rutherford a alors imaginé un atome presque complètement vide sauf pour un minuscule noyau positif autour duquel des électrons tournent dans un immense nuage. L'atome étant principalement vide, cela donne tous l'espace nécessaire au passage en ligne droite de la plupart des particules alpha, sauf pour les quelques unes qui passent près d'un noyau d'atome d'or qui sont déviées. Mais comment un noyau minuscule peut-il contenir un grand nombre de protons positifs sans que ceux-ci se repoussent mutuellement? Rutherford a conclu qu'il devrait un avoir une autre particule, neutre, que personne n'a encore découvert. Il appela cette particule le neutron dont l'existence fut observée seulement plusieurs années plus tard, dans les années 1930. La masse des protons et des neutrons est à peu près égale, mais celle des électrons est beaucoup plus petite. En 1911, Rutherford présente son modèle de l'atome. (animation flash de l'expérience de la feuille d'or) |
Ressources
|
|
|
Découverte des différents éléments sur Les éléments chimiques.