Les propriétés physiques de la matière
- On utilise le cuivre dans les fils électriques car c'est un excellent conducteur d'électricité
- On utilise les propriétés des bases pour neutraliser les acides dans un cas de mal d'estomac
- Le caoutchouc est utilisé comme isolant électrique et pour améliorer l'adhérence
- La friabilité du graphite des mines de crayons permet de tracer des lignes et d'écrire sur différentes surfaces
- Le magnétisme de certaines matières permet de produire de l'électricité
- Aucun composant électronique n'existerait sans les propriétés semi-conductrices des métalloïdes, principalement du silicium.
Masse volumique
Il existe plusieurs manières de décrire la matière. On peut donner la couleur, le lustre, la conductivité électrique, etc. Toutes ces propriétés servent à reconnaître (identifier) la matière. Parmi les propriétés, la masse volumique est très souvent utilisée en sciences.
La masse volumique est le rapport entre la masse d’un échantillon de matière et son volume. Ce rapport reste le même peu importe la taille de l’échantillon. Par exemple, chaque cm3 de cuivre a une masse de 8,95 g. On dit que sa masse volumique est de 8,95g/cm3. Ceci signifie que 2 cm3 de cuivre a une masse de 17,90g, soit deux fois plus de masse; et 10 cm3 de cuivre a une masse de 89,5g. Le rapport entre la masse du cuivre et son volume calculé en g/cm3 reste toujours de 8,95g/cm3.
Ce qui rend la propriété de masse volumique particulièrement intéressante pour les chimistes est que les matières ont une masse volumique presqu’unique. Par exemple, très peu de matières ont une masse volumique de 8,95g/cm3. Si on calcule la masse volumique d’un échantillon de matière inconnue, et qu’on obtient 8,95g/cm3, cela élimine presque toutes les matières sauf quelques-unes dont le cuivre. La masse volumique permet presque d’identifier une matière inconnue. En ajoutant quelques autres observations, la couleur, le reflet de lumière, la conductivité électrique, etc., on peut identifier un matière inconnue.
Bref, la masse volumique est une propriété souvent utile pour identifier des substances. Chaque substance a sa propre masse volumique différente de toutes les autres ou presque. Comme le nom l'indique, la masse volumique est le rapport entre la masse et le volume d'une substance.
|
Notes et exercices corrigés sur l'identification de la matière à l'aide de la masse volumique
|
| ||||||
Les atomes dans la matière sont en mouvement constant. Selon l'énergie qui se trouve dans la matière, le mouvement des atomes est soit libre, dans toutes les directions, soit une simple vibration très restreinte ou soit entre les deux. Plus on ajoute de l'énergie aux atomes, plus leur mouvement s'intensifie. En réduisant l'énergie, le mouvement des atomes se restreint.
Ces ce mouvement des atomes qui détermine dans quelle phase se trouve la matière :
- La matière est un solide lorsque ses atomes ont un mouvement très restreint, une vibration.
- La matière est un liquide lorsque ses atomes ont un plus grand mouvement, mais sans beaucoup de liberté.
- La matière est un gaz lorsque ses atomes ont une grande liberté de mouvement et qu'ils se déplacent dans toutes les directions.
Chaque matière change de phase (solide à liquide, liquide à gaz, et vis versa) à des températures précises. L'eau, par exemple, passe de l'état solide à liquide ou liquide à solide à 0°C. L'eau passe de l'état liquide à gazeux ou gazeux à liquide à 100°C.
On appelle point de fusion la température à laquelle une substance passe de l'état solide à liquide. Le point de fusion de l'eau est de 0°C, celui du mercure est de -39°C et celui de la cire d'abeille est autour de 63°C.
On appelle point d'ébullition la température à laquelle une substance passe de l'état liquide à l'état gazeux. Le point d'ébullition de l'eau est de 100°C, celui de l'éthanol est de 78,4°C et celui du dioxyde de carbone est de -78,5°C.
Les température de fusion et d'ébullition sont mesurés à pression normale. En augmentant la pression, les points de fusion et d'ébullition deviennent plus élevés puisqu'il faut plus d'énergie pour que les atomes puissent augmenter leur mouvement.
On utilise les propriétés de points de fusion et de points d'ébullition pour séparer des substances en solution par le processus de distillation. Par exemple, les différents points d'ébullition des gaz de l'air nous permettent d'en extraire l'argon, l'oxygène, de gaz carbonique et l'azote.
|
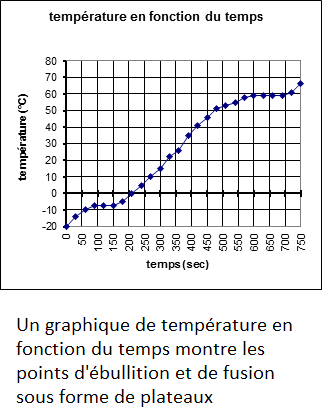
Interprétation de graphiques de température en fonction du temps
En chauffant une substance à partir de son état solide, on peut mesurer sa température en fonction du temps. On remarque alors que les températures arrêtent d'augmenter temporairement lorsque la substance atteint ses points de fusion et d'ébullition. Cet effet de plateau permet d'identifier les points de fusion et d'ébullition de manière graphique. Le graphique à droite montre que la température de l'échantillon d'une substance était de -20°C au moment où on a commencé à la faire chauffer. lorsque la température atteint -8°C à -7°C, la température ne change plus pendant plus de 50 secondes. À ce moment, la substance passe de l'état solide à l'état liquide et ce changement absorbe toute la chaleur qui est ajouté de manière à ce que les atomes augmentent leur mouvement. Le point de fusion de cette matière est donc autour de -8°C. Vers 150 secondes, la température recommence à monter. la substance est maintenant complètement liquide. Après 600 secondes, on remarque que la température atteint un nouveau plateau juste au-dessous de 60°C. La substance passe maintenant à l'état de gaz. Le point d'ébullition est donc d'environ 60°C. Avec ces renseignements, on peut faire une recherche d'une matière dont les points de fusion et d'ébullition sont respectivement de 8°C et de 60°C. Le brome semble un bon candidat avec un point de fusion de -7,2°C et un point d'ébullition de 58,8°C |
Fiches signalétiques
- Identification du produit chimique et de la compagnie
- Composition/information sur les ingrédients
- Identification des risques
- Premiers soins
- Lutte contre les incendies
- Marche à suivre en cas de dispersement accidentelle
- Manutention et entreposage
- Contrôle de l'exposition/protection individuelle
- Propriétés physiques et chimiques
- Stabilité et réactivité
- Information toxicologique
- Information écologique
- Élimination du produit
- Information sur le transport
- Information sur la réglementation
- Renseignements divers
Étiquetage
En plus des fiches signalétiques, les contenants des produits présentent des symboles avertissant des risques d'utilisation. Voici une affiche du SIMDUT (Système d'information sur les matières dangereuses utilisées au travail) présentant les pictogrammes symboliques pour chaque catégorie de danger.